Tus compañeros, la silla en la que te sientas, o el aire que respiras están formados por materia.
La música que oyes, la luz que te permite ver o las ideas que se te ocurren, por el contrario, son inmateriales, no están hechas de materia.
Un perro, los lápices o el pupitre están hechos de materia, pero son totalmente distintos porque están hechos de clases de materia distinta.
No toda la materia es igual.
Cada clase de materia se llama sustancia y varias materias diferentes forman una mezcla.
Por ejemplo, una ensalada sería una mezcla formada por varias sustancias diferentes.
Pero primero veamos qué es la materia y como se calcula y al final veremos su propiedades.
Indice de Contenidos
¿Qué es la Materia?
Es todo aquello que tiene masa y ocupa volumen.
Así de sencillo, por eso cuando empezamos el tema decíamos que un lápiz, el aire, el humo es materia, pero la música y los sentimientos NO.
Una vez que tenemos claro lo que es la materia profundicemos un poco mas en ella.
¿Cómo se Mide?.
Fácil tenemos que medir su masa y su volumen.
Medimos la Masa
¿Cómo medimos la masa de la materia?
Respuesta sencilla, con una balanza.
Un poco más complicado es calcular el volumen, ya que depende de su estado. Veamos como se calculan los volúmenes.
Calculamos el Volumen
Volúmenes en los Líquidos
En este caso se calcula con la ayuda de una probeta graduada en cm3 (centímetros cúbicos) ,m3, etc. o bien mediante unidades de capacidad como el litro, decilitro, etc.
Recordamos que la capacidad es una magnitud solo utilizada en los líquidos para calcular su volumen y que por lo tanto tiene equivalencia con la medida del volumen en general.
Veamos alguna equivalencia: 1dm3=1Litro (L) y 1cm3= 1 mililitro (mL).
Volúmenes en Solidos
En este caso depende del sólido que estemos hablando.
Sólidos Regulares: Son aquellos que tienen una forma que permite calcular su volumen mediante una formula.
Por ejemplo un cubo es regular y la formula para calcular su volumen es V= lado x lado x lado.
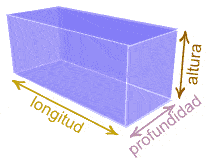
Otro ejemplo seria un prisma rectangular (caja de cerillas) su formula serie V= Largo x ancho x profundidad.
Hay muchos más como por ejemplo la esfera es V =4/3 x π x radio3.
Solidos irregulares: Los que no tienen forma definida, por ejemplo una piedra.
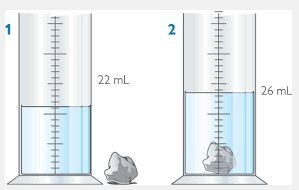
En este caso hay que disponer una probeta con un líquido inicial. Se anota su volumen inicial.
Posteriormente se introduce el solido irregular y el volumen que marca la probeta aumenta (tanto como el volumen que ocupa el solido).
La diferencia entre el volumen inicial y el final es precisamente el volumen del sólido.
En el ejemplo de la imagen el volumen de la piedra sería se 4mL (mililitros).
Si la probeta está regulada en centímetros cúbicos obtendríamos el volumen en esta unidad.
Volúmenes en Gases
¿Y el volumen en los gases?
Pues los gases no tienen un volumen definido ya que se adaptan al recipiente que lo contienen.
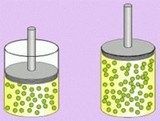
Por ejemplo un gas dentro de una botella de 1cm3 tiene el mismo volumen que la botella 1cm3, pero si ese mismo aire lo introducimos en una botella de 3cm3 el aire se adapte a la botella ocupando todo el volumen nuevo, es decir ahora su volumen será de 3cm3.
Por lo tanto el volumen de un gas es el mismo que el volumen del recipiente que lo contiene.
El mismo gas puede ocupar volúmenes diferentes.
El Aire es Materia
Primera pregunta:
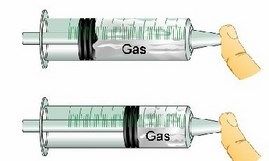
Haz la prueba, coge una jeringuilla tapa el saliente y aprieta, verás que no puedes llegar al final por que al tener aire dentro, este ocupa un volumen.
Por la tanto si que tiene volumen.
¿Y masa?
Pesa una botella con aire, ahora introduce aire a presión dentro de ella y verás como ahora pesa más.
¿Por qué?
Por que tiene más aire, por lo tanto el aire tiene masa. ES MATERIA.
Si quieres saber más sobre medidas de volumen te puede interesar: Instrumentos Para Medir Volumen.
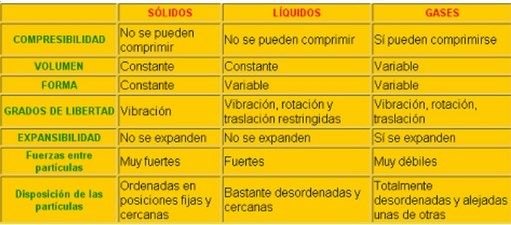
Forma, Volumen, Dilatación y Atracción de sus Moléculas
Vamos ahora a ver como se comporta en sus 3 estados diferentes en cuanto a si tiene o no forma definida, como es su volumen, como se dilata y como es la fuerza de atracción de sus moléculas en cada uno de los 3 estados.
El estado de agregación es como se llama a los diferentes estados posibles de la materia: solido, líquido y gaseoso.
Vamos hablar un poco más sobre la atracción de las moléculas en la materia en sus 3 estados.
Fuerza de atracción Molecular en la Materia
La materia esta formada por átomos o por moléculas (varios átomos).
Nosotros vamos a representar a las moléculas y a los átomos mediante esferas.
Las moléculas y los átomos de la materia se encuentran unidos unos con otros mediante una fuerza llamada fuerza de atracción intermolecular.
Esta fuerza cambia dependiendo del estado en que se encuentre la materia.
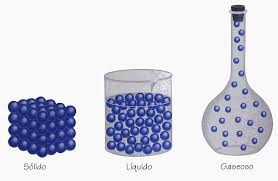
Fíjate como están las moléculas en cada estado:
Sólido: Las moléculas tienen una gran fuerza de atracción entre ellas y están muy unidas, no pueden moverse, es por eso que los solidos tienen forma definida
¿Qué pasa si calentamos el sólido?
Pues hacemos que esta fuerza de atracción disminuya y las moléculas se separen hasta que llega un momento en que el solido se convierte en líquido.
El calor cedido al cuerpo solido se emplea en disminuir las fuerzas de atracción molecular y en separar las moléculas unas de otras.
En los líquidos: Las moléculas tienen una fuerza de atracción entre ellas menor que en los sólidos y tienen cierto movimiento, es por eso que los líquidos no tienen una forma definida.
En los Gases: Al dar calor al liquido, este calor hace que se separen mas las moléculas y ya casi no tengan atracción entre ellas moviéndose libremente a gran velocidad, es por eso por lo que los gases se expanden invadiendo todo el recipiente.
¿Solo tiene 3 estados posibles la materia?
La respuesta es No. Hay un cuarto estado llamado PLASMA.
Este estado lo alcanza la materia cuando está ha grandes temperaturas, y se diferencia del gaseoso por que en este estado la velocidad de los átomos es tan grande que al chocar entre ellos y por la elevada temperatura se liberan electrones quedando en forma de Iones + y con un movimiento a una gran velocidad y sin orden aparente.
Este estado no es muy estudiado pero resulta que en el universo (no en la tierra) el 99% de la materia esta en estado de plasma.
Esto es como esta la materia por ejemplo del sol y de la mayoría de las estrellas.
Si quieres saber más sobre este estado visita este enlace: Estado Plasma.
Últimamente es más famoso por las televisiones con pantallas de plasma, en cuyo interior encontramos gases que se encuentran en este estado.
En estado de plasma la materia es un gran conductor eléctrico.
Cambios de Estado de la Materia
Como ya hemos visto al aumentar la temperatura (y a presión constante) la materia cambia de estado.
Pero cada materia diferente necesita una temperatura diferente para que cambie de estado.
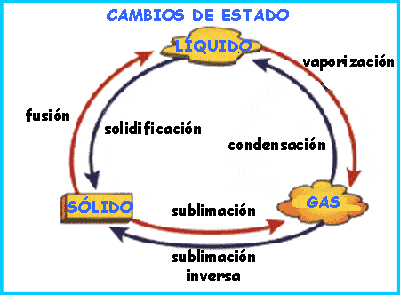
Primero veamos como se llaman los diferentes cambios de estado de la materia:
Como decíamos cada tipo de materia diferente cambia de estado a temperaturas diferentes, pero las temperaturas a las que cambian de estado se llaman igual:
Temperatura de fusión-solidificación: Temperatura a la que pasa de sólido a líquido.
Esta temperatura es la misma a la que pasa de liquido a sólido pero se llama temperatura de solidificación.
Si el cuerpo esta en estado solido y lo llevamos a la temperatura de fusión y seguimos dándole calor, este calor se utilizará para pasarlo de solido a líquido, no para aumentar la temperatura del sólido, una vez que todo el sólido esta convertido en líquido y seguimos dándole calor, ahora ese calor si que se utiliza para elevar la temperatura pero del líquido.
Si la materia está en estado líquido y el líquido lo ponemos a la temperatura de solidificación o fusión ( es la misma) y lo enfriamos este frio no hace que baje la temperatura del líquido sino que se emplea para el paso de liquido a sólido (Temperatura de solidificación).
La temperatura de fusión o de solidificación, que es la misma de un tipo de materia, se llama su punto de fusión.
Cada materia diferente tiene su propio punto de fusión.
Temperatura de ebullición-condensación: Temperatura a la que la materia pasa de estado liquido a gas (ebullición) o de gas a líquido (condensación).
Estos cambios de estado se hacen de la misma forma que los anteriores suministrando calor o frio.
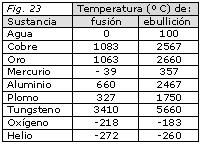
Cada materia tiene un punto de ebullición diferente. Veamos ahora los diferentes puntos (temperaturas) a los que diferentes tipos de materia cambian de estado:
Como vemos cada tipo de materia diferente tiene sus propios puntos de fusión y ebullición y es exclusiva de ella.
Si tenemos en una caja con un tipo de materia y para averiguarla damos una pista como que su punto de fusión es de-39ºC.
¿Cuál sería?
Pues solo podría ser el Mercurio.
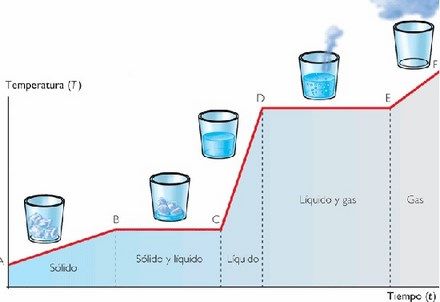
El punto D sería para 100ºC en el caso del agua.
Fíjate que durante un tiempo suministramos calor al agua a 100ºC para que pase todo el líquido a gas (desde D hasta E).
Conviven en los dos estados.
En el punto E ya tenemos todo el líquido convertido en gas.
Lo mismo ocurre para pasar de líquido a sólido a 0ºC.
Empezaría la conversión en el punto C (0ºC) y en D ya tendríamos todo el líquido en estado sólido.
Puedes saber más sobre los cambios de estado en el siguiente enlace: Cambios de Estados de la Materia.
Propiedades de la Materia
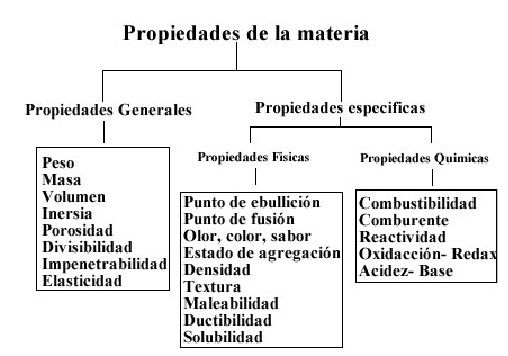
La materia tiene propiedades y son las que hacen que podamos diferenciar unas de otras, pero hay dos tipos de propiedades específicas y generales.
Propiedades específicas: Son aquellas propiedades que permiten diferenciar un tipo de materia de otra.
Estas propiedad son diferentes para cada tipo de materia, por eso podemos diferenciarla.
Como ya dijimos por ejemplo la temperatura de fusión será una propiedad específica, ya que cada materia tiene una diferente, a 0ºC solo puede ser agua pura.
También lo es la densidad, ya que cada tipo de materia tiene densidad diferente.
Propiedades Generales: Son aquellas que no sirven para diferenciar un tipo de materia de otra.
Por ejemplo la masa, ya que hay muchos tipos de materia que pueden tener la misma masa o que sea conductor eléctrico, etc.
Sin embargo, tenemos que tener en cuenta, que puede ser que varias propiedades generales identifiquen un tipo de materia.
Densidad: Ligeros y Pesados
La densidad es una propiedad específica de la materia, cada materia tiene su propia densidad= masa/volumen.
La densidad de un material nos da una idea de lo ligero o pesado que es el material.
Altas densidades son cuerpo pesados, y bajas densidades las tienen los cuerpos ligeros.
Por ejemplo el plomo tiene una densidad de 11,35g/cm3 y la del corcho es de 0,24g/cm3.
Esta claro cual es ligero y cual es pesado.
También es muy importante la densidad para la flotabilidad (saber si un cuerpo flota sobre otro) ya que un cuerpo flotará sobre otro si es menos denso.
Por ejemplo la densidad del agua es de 1g/cm3.
Esta claro que el corcho flotará sobre el agua pero no el plomo.
La densidad también nos da una idea del volumen que ocupan los cuerpos.
Por ejemplo, según la fórmula de la densidad para tener bastante peso de corcho esta claro que necesitamos mucha cantidad (volumen) de corcho, y sin embargo mucha cantidad de plomo ocupara poco volumen.
No olvidemos que el volumen es inversamente proporcional a la masa en la fórmula.
A todos nos han preguntado alguna vez ¿ es más pesado un kilo de plomo o uno de paja?, y muchos nos hemos equivocado y hemos respondido que el kilo de plomo, sin advertir que, en ambos casos, se trata de un kilo.
Y es que un kilo de plomo ocupa mucho menos volumen que un kilo de paja y, por eso, decimos que es más pesado.
Para hablar con propiedad, debemos decir que el plomo es más denso que la paja, es decir, que una misma masa, tiene menos volumen.
Ejercicios sobre la Materia
Por último te dejamos unos ejercicios para que repases lo aprendido.
1ª) ¿Qué es la materia?
2ª) Explica como se mide el volumen en los 3 estados diferentes de la materia.
3ª) Haz una tabla con los estados de agregación y como se comportan en cuanto a la forma, el volumen, la dilatación y la fuerza interacción de las moléculas en cada uno de los estados.
4ª) ¿Cómo esta la materia en estado de plasma?
5ª) Haz un esquema con los cambios de estado de la materia.
6ª)¿Qué es el punto de fusión de un material? ¿Y el de ebullición?
7ª) Define propiedades especificas y generales de la materia con dos ejemplo de cada una de ellas.
8ª) Materia ligera o pesada. Flotabilidad. Explica que tiene que ver esto con la densidad.
9ª) Haz las gráficas de los cambios de estado del alcohol y del mercurio.
10ª)¿En qué estado esta el hierro a 1500ºC? ¿Y el mercurio?.
Tienes más ejercicios para hacer online en este enlace: Ejercicios Materia.
También Te Puede Interesar:
–Niveles de Organización de la Materia
Si te ha gustado la página sobre la Materia pulsa en Compartir. Gracias
© Se permite la total o parcial reproducción del contenido, siempre y cuando se reconozca y se enlace a este artículo como la fuente de información utilizada.