Las fuerzas de Van der Waals se llaman así en honor al físico holandés Johannes Van der Waals.
Estas fuerzas son las responsables de muchos fenómenos físicos y químicos como la adhesión, rozamiento, difusión, tensión superficial y la viscosidad.
Vamos a explicar fácilmente para que se entienda lo que son las fuerzas de van der waals, los tipos que hay (dipolo-dipolo, dipolo-dipolo inducido y fuerzas de london), su importancia y por último la ecuación de van der waals.
Indice de Contenidos
¿Qué son las Fuerzas de Van Der Waals?
Lo primero que tenemos que saber es que las sustancias químicas están formadas por moléculas compuestas de átomos, unidos entre si por medio de enlaces químicos (covalente, iónico o metálico).
La energía almacenada por estos enlaces, sumada a la red molecular de todo el conjunto de moléculas que forma la sustancia, determina la estabilidad de estos enlaces.
Piensa que si en varias moléculas, por ejemplo unidas con enlaces covalente, no hubiera ninguna fuerza de unión entre ellas, estarían moviéndose libremente y por lo tanto siempre estarían en estado gaseoso (movimiento libre de las moléculas).
Ya sabemos que eso no es así, por que pueden estar también en estado sólido o líquido (no se mueven libremente), y esto quiere decir que habrá algún tipo de conexión-unión entre las moléculas.
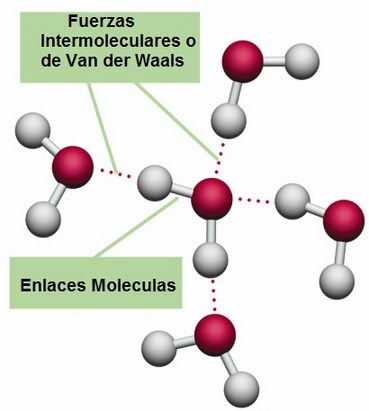
Ha este tipo de interacción o fuerza es lo que se conoce como fuerzas de interacción intermoleculares o de van der Waals.
Las fuerzas de van der Waals son fuerzas de estabilización molecular (dan estabilidad a la unión entre varias moléculas), también conocidas como atracciones intermoleculares o de largo alcance y son las fuerzas entre moléculas (fuerzas entre molecula-molecula).
Son fuerzas mas débiles que las internas que unen la molécula ya que dependen exclusivamente del tamaño y forma de la molécula pudiendo ser de atracción o de repulsión.
Son tan débiles que no se las puede considerar un enlace, como el enlace covalente o iónico, solo se las considera una atracción.
Para tener una idea de la poca fuerza que tienen, si un enlace covalente tuviera una fuerza de 100, las de Van der Waals serían de valor 1 (100 veces menor).
De hecho las fuerzas de van der Waals son las fuerzas atractivas o repulsivas entre moléculas (o entre partes de una misma molécula)distintas a aquellas debidas a un enlace (covalente, iónico o metálico).
Incluyen a atracciones entre átomos, moléculas y superficies fuera de los enlaces normales.
Antes de explicar cada una de los tipos de fuerzas posibles de Van der Waals es importante conocer que hay moléculas polares y no polares.
Moléculas Polares y NO Polares
Moléculas Polares son aquellas cuyos enlaces son formados por átomos distintos con grandes diferencias de electronegatividad, formando moléculas polares.
La molécula es eléctricamente neutra en su conjunto por tener igual de partículas positivas y negativas, pero no existe simetría en la distribución de la electricidad.
La distribución de las cargas eléctricas no es simétrica respecto a un centro.
Las moléculas están formadas por átomos diferentes y la carga eléctrica está más concentrada en una zona de la molécula que en otra.
En este caso ocurre igual que en una pila, se forman polos eléctricos, con una pequeña carga negativa y otra positiva separadas, por eso se llaman polares.
Aquellas en las que no hay esa diferencia de zonas eléctricas positiva y negativa en la molécula se llaman NO polares.
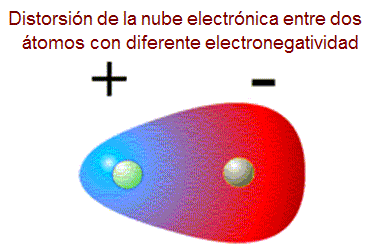
Las moléculas polares tienen distorsionada su nube electrónica con respecto a su centro.
Este tipo de moléculas, las polares, tiene lo que se llama un dipolo permanente, es decir es como un imán pequeñito pero molecular, por eso, la parte negativa atraerá a la zona positiva de otras moléculas cercanas y viceversa.
Ejemplos de moléculas Polares: Agua H2O , Amoníaco NH3 , Fluoruro de Hidrógeno HF , Fosfina PH3 , Cloformo CHCl3.
Moléculas NO Polares o también llamadas Apolares: Cuando se forman en un enlace covalente entre átomos iguales, la molécula es neutra, es decir, tiene carga eléctrica cero.
Estas moléculas no tienen esas zonas de carga eléctrica separadas y por lo tanto no forman dipolos permanentes.
Ejemplos de Moléculas No Polares: Tetracloruro de Carbono CCl4 , Dióxido de Carbono CO2 , Cloro Cl2 , Trióxido de Azufre SO3 , Hidrógeno H2.
Resumiendo, las MOLÉCULAS POLARES son las que tienen una zona con una pequeña carga negativa y otra zona con una pequeña carga positiva. (la parte negativa atraerá a la zona positiva de otras moléculas y viceversa).
Las MOLÉCULAS NO POLARES son las que no tienen esas zonas de carga eléctrica separadas.
¿Cómo saber si una sustancia es polar o no?
Hay una forma sencilla, que nos vale para la mayoría de casos.
LOS DISOLVENTES POLARES DISUELVEN A SUSTANCIAS POLARES, LOS DISOLVENTES APOLARES A SUSTACIAS APOLARES.
La regla química de que «lo semejante disuelve a lo semejante». Es decir, ya sabemos que el agua es un disolvente polar. Si echas en ella azúcar, ¿se disuelve?…si ¿verdad?. Pues ya sabes que el azúcar sería una sustancia Polar.
Pero, ¿y si echas aceite en el agua?. El aceite queda flotando, no se disuelve en el agua. Por tanto el aceite sería una sustancia No Polar.
Tipos de Fuerzas de Van der Waals
Ahora que ya sabemos que hay moléculas polares y no polares explicaremos los 3 tipos de fuerzas diferentes de van der Waals que pueden darse entre moléculas.
DIPOLO-DIPOLO: Cuando dos moléculas polares (dipolo) se aproximan, se produce una atracción entre el polo positivo de una de ellas y el negativo de la otra.
Se forma entre un dipolo positivo de una molécula polar con el dipolo negativo de otra polar.
Una atracción dipolo-dipolo es una interacción no covalente entre dos moléculas polares.
Las moléculas que son dipolos se atraen entre sí cuando la región positiva de una está cerca de la región negativa de la otra.
Podríamos decir que es similar al enlace iónico pero mucho más débil.
Esta fuerza de atracción entre dos dipolos es tanto más intensa cuanto mayor es la polarización de dichas moléculas polares.
Ejemplos podrían ser el sulfuro de hidrógeno H2S , el metanol CH3OHy la glucosa C6H12O6.
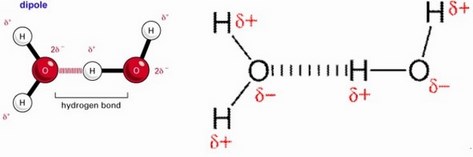
Los Puentes de hidrógeno es un tipo especial de interacción dipolo-dipolo entre el átomo de hidrógeno que está formando un enlace polar, tal como N—H, O—H, ó F—H, y un átomo electronegativo como O, N ó F.
Interacciones Iónicas o Dipolo-Dipolo Inducido
En ciertas ocasiones, una molécula polar (dipolo), al estar próxima a otra no polar, induce en ésta un dipolo transitorio, produciendo una fuerza de atracción intermolecular llamada dipolo-dipolo inducido o interacción iónica.
Son interacciones que ocurren a nivel de catión-anión, entre distintas moléculas cargadas, y que por lo mismo tenderán a formar una unión electrostática entre los extremos de cargas opuestas debido a la atracción entre ellas.
Un ejemplo: El agua cuya molécula es un dipolo, produce una pequeña polarización en la molécula no polar de oxígeno, la cual se transforma en un dipolo inducido.
Esto hace que el oxígeno y el dioxido de carbono, que son no polares presenten cierta solubilidad en solventes polares, como el agua.
Fuerzas de London o Dispersión
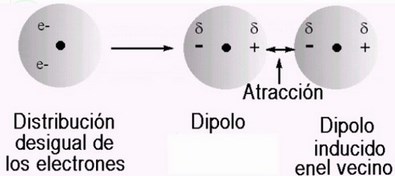
En las moléculas no polares puede producirse transitoriamente un desplazamiento relativo de los electrones, originando un polo positivo y otro negativo (dipolo transitorio) que determinan una atracción entre dichas moléculas (el polo positivo de una molécula atrae al polo negativo de la otra, y viceversa).
Son dipolos instantáneos, desaparecerán en muy poco tiempo.
Pensemos en una molécula como en algo no estático, sino en movimiento, pero además conteniendo electrones en constante movimiento.
Es razonable pensar que en un determinado momento la distribución en esa molécula puede no ser perfectamente simétrica y aparecen entonces pequeños dipolos instantáneos en este momento.
Estas fuerzas de atracción son muy débiles y se denominan fuerzas de London. Las fuerzas de London se presentan en todas las sustancias moleculares.
Son el resultado de la atracción entre los extremos positivo y negativo de dipolos inducidos en moléculas adyacentes.
En general, cuantos más electrones haya en una molécula más fácilmente podrá polarizarse. Así, las moléculas más grandes con muchos electrones son relativamente polarizables.
En contraste, las moléculas más pequeñas son menos polarizables porque tienen menos electrones.
Importancia de las Fuerzas de Van der Waals
Gracias a ellas podemos explicar la adhesión, el rozamiento, la difusión, la tensión superficial y la viscosidad.
Por ejemplo, sabemos porque la nafta es liquida, el metano es un gas y el polietileno (que es un polímero compuesto por C y por H únicamente) es un solido.
Las fuerzas de Van der Waals, aún siendo tan débiles, definen el carácter químico de muchos compuestos orgánicos.
Ecuación de Van der Waals
Van der Waals introdujo correcciones a la ecuación de estado de un gas ideal, que tenían en cuenta el volumen finito de las moléculas y las fuerzas atractivas que una molécula ejercía sobre otra a distancias muy cercanas entre ellas.
Si te interesa:
Vídeo Fuerzas de Van der Waals
Por último te dejamos un vídeo que explica las fuerzas de Van der Waals por si todavía no lo tienes claro:
Si te ha gustado pulsa en Compartir. Gracias
© Se permite la total o parcial reproducción del contenido, siempre y cuando se reconozca y se enlace a este artículo como la fuente de información utilizada.